本文来自动脉网网站(https://www.vbdata.cn/)
作者:车维维
信销网经授权发布
作者:车维维
信销网经授权发布
2023年刚刚过去,迎来了崭新的2024年。
过去一年来,尽管生物医药产业仍面临诸多变化和挑战,但产业致力于为全球病患带来创新疗法的脚步始终在向前。
尽管当前资本市场的寒意仍未过去,FDA在2023年批准新药数量却创下五年新高。这对于目前寒冷的医药行业来说是一剂强心针,为药物研发和医疗行业以及患者带来了巨大的希望。
FDA获批的创新药是全球创新药物研发动态的方向标,为创新药企引领方向。基于此,本文对2023年FDA批准新药进行了盘点和梳理。
69款新药获批,小分子药物数量瞩目
截止至2023年12月28日,2023年FDA共批准了69款新药,数量创5年新高。
其中,FDA旗下的药物评估和研究中心(CDER)批准了55款创新药,具有创新机制的疗法占比超过六成。其中17款生物制品,9款获得孤儿药指定;38款新分子实体,20款获得优先审评,16款获得孤儿药指定。
生物制品评估和研究中心(CBER)批准了14款生物制品(不含血液制品和筛选试剂),分别为5款疫苗、5款基因治疗产品(其中包含全球首个获批的CRISPR基因编辑疗法Casgevy)、2款细胞治疗产品,以及首款口服粪便微生物群产品Vowst。
分析2023年FDA批准新药类型,小分子药物数量引人瞩目。小分子药物作为医药领域的主力之一,获批数量在所有药物类型当中位居榜首,共有25款小分子药物获批,占比达到36%。
其次是大分子药物,共有14款获批,数量居第二,占比为20%。
值得一提的是,多肽类和核酸类药物的新分子疗法占比近10%,成为重要的新药来源。
罕见病收获榜首,肿瘤仍是重点领域
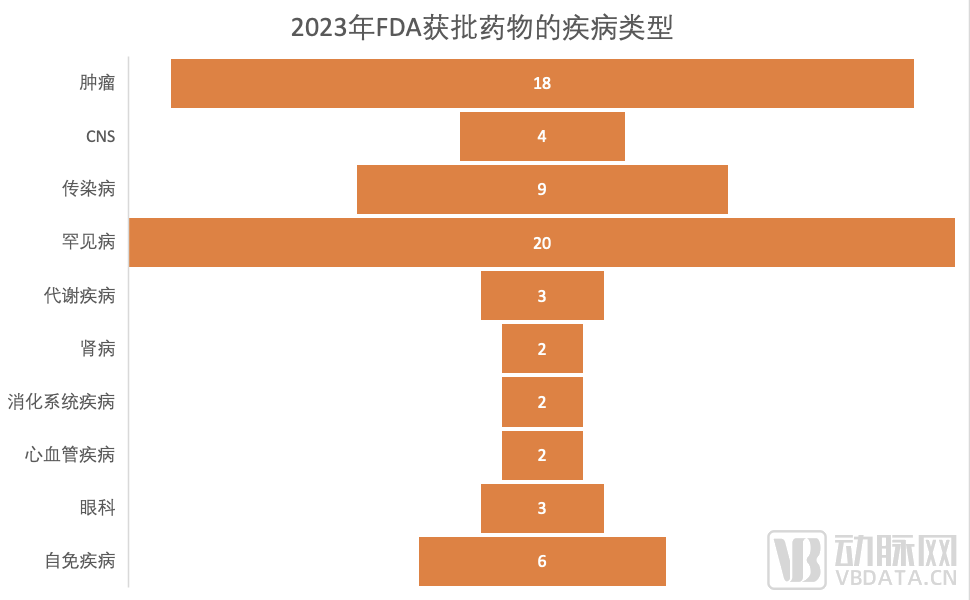
对2023年FDA批准药物的疾病领域进行分析,获批新药适应症呈现出百花齐放趋势,其中罕见病和肿瘤仍是重点领域。

值得一提的是,2023年是罕见疾病收获颇丰的一年,有20款罕见病新药获批上市,高居2023年FDA批准新药疾病领域的首位。
诸多遗传性免疫缺陷性疾病患者迎来新的治疗选择,比如α-甘露糖苷贮积症、法布里病、弗里德赖希共济失调、雷特综合征、绝经引起潮热、成人骨髓纤维化伴贫血、成年晚发型庞贝病、1型原发性高草酸尿症、大疱性表皮松解症等等。
据了解,CDER在过去的2022年批准的37款新药中,仅有5款为孤儿药。2023年这一数字的上升,也说明了FDA对于罕见病领域的关注在逐步上升。
在FDA批准药物的疾病领域中,肿瘤领域的产品为18款,位列第二。细分领域包括套细胞淋巴瘤、乳腺癌、默克尔细胞癌、弥漫性大B细胞淋巴瘤、多发性骨髓瘤、鼻咽癌、ROS1阳性非小细胞肺癌、HR+/HER2-乳腺癌和侵袭性纤维瘤病等等。
不仅如此,在传染病、自免、CNS以及代谢等疾病领域也有多款重磅产品问世。
MNC占比近半,辉瑞狂扫9款,联合申报成常态
再看获批药物的公司类型。今年 CDER 和 CBER 批准的创新疗法中,可以看到MNC和上市Biopharma为申报主力。其中31款新药源自MNC,位列榜首;18款新药来自上市Biopharma,位列第二。
更值得注意的是,在获批药物的申报公司中,Biotech的身影更加频繁,更有超半数的新分子疗法来源于小型生物技术公司。可以说,新兴生物医药公司已成为重要创新来源。
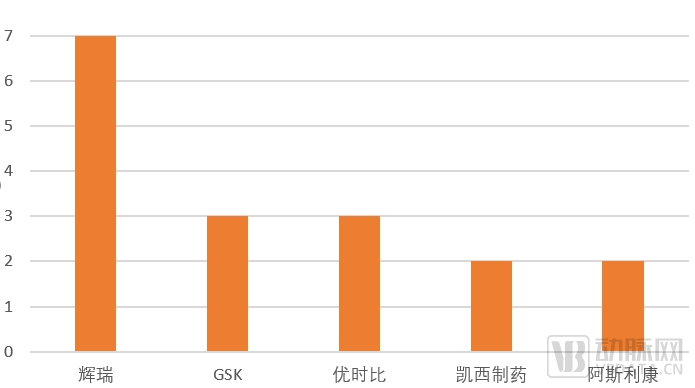
进一步看获批公司,2023年FDA新药申报的最大赢家当属辉瑞Pfizer,共获批9款新药,其中包括4个NME,1个双抗,1个生长激素,3个疫苗。
其次为优时比以及葛兰素史克,分别获批3款新药。凯西制药和阿斯利康则分别获批2款新药。
在2023年FDA批准的69款新药中,有11款是两家企业联合申报、或联合研发的情况。这也预示着,未来新药联合研发、联合申报将成为新常态。
2023年FDA重磅新药:多款FIC疗法,国产3款获批
2023年,FDA批准新药中包括多款“first-in-class”疗法,例如20年来FDA第一款完全批准的阿尔茨海默症新药Lecanemab,FDA首款弥漫性大B细胞淋巴瘤(DLBCL)双特异性抗体pcoritamab,FDA批准的首个治疗产后抑郁症(PPD)的口服药物Zuranolone等等。
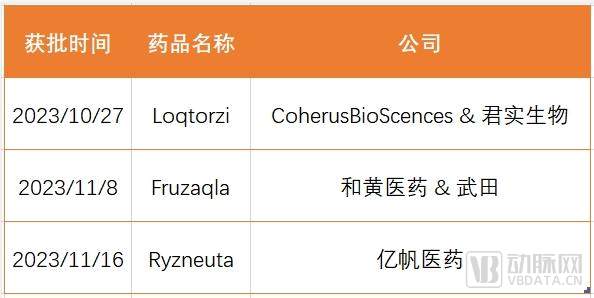
与此同时,观察国内创新药企,2023年也有3家中国药企创新药获得FDA批准,分别为亿帆医药的Ryzneuta、和黄医药的Fruzaqla与君实生物的Loqtorzi。

截止目前,国内已有五款国产创新药产品在美获批,主要包括百济神州的泽布替尼(2019年11月14日在美国取得全球首次批准)、传奇生物的Carvykti(2022年3月获批)、和黄医药的呋喹替尼、亿帆医药的艾贝格司亭α注射液,以及君实生物的特瑞普利单抗。
以下为本文列举的2023FDA十大重磅药物:
>>>>20年来首款FDA完全批准AD新药:Leqembi
1月6日,渤健/卫材的抗β淀粉样蛋白(Aβ)单抗Leqembi(lecanemab)获FDA加速批准上市,用于治疗阿尔茨海默症(AD)。7月6日,FDA同意将加速批准转为完全批准。这意味着lecanemab成为了20年来首款获得FDA完全批准的AD新疗法。Lecanemab能够选择性结合以中和消除可溶性、有毒的Aβ聚集体(原纤维),而这些聚集体被认为有助于AD中的神经退行性过程。III期关键研究显示,lecanemab不仅能降低淀粉样蛋白斑块,患者临床痴呆症状也可显著得到改善。
>>>>首款非共价BTK抑制剂:Jaypirca
1月27日,礼来的Jaypirca(pirtobrutinib, 100mg和50mg片剂)获FDA加速批准上市,用于既往接受过至少二线系统治疗的复发或难治性套细胞淋巴瘤(MCL)成人患者,包括布鲁顿酪氨酸激酶(BTK)抑制剂,这是FDA批准的首个也是唯一一款非共价(可逆)BTK抑制剂。Jaypirca既能抑制野生型也能抑制C481S突变型BTK,可以在既往使用共价BTK抑制剂(包括伊布替尼、阿卡替尼或泽布替尼)治疗的MCL患者中重建BTK抑制,并延长靶向BTK途径的益处。
>>>>首款治疗FA的药物:Skyclarys
2月28日,FDA批准Reata Pharmaceuticals的Skyclarys(omaveloxolone)上市,用于治疗16岁及以上青少年和成年人弗里德赖希共济失调症(Friedreich’s Ataxia,FA)。这是美国首个也是唯一获批治疗FA的药物。今年7月底,渤健以每股172.5美元的价格现金收购Reata,交易总额约为73亿美元。Omaveloxolone是一款每日口服一次的Nrf2激动剂。Nrf2是一种转录因子,通过恢复线粒体功能、减少氧化应激和抑制促炎信号来促进炎症消退。
>>>>首款治疗ALS的基因靶向疗法:Qalsody
4月25日,渤健/Ionis联合推出的反义寡核苷酸疗法Qalsody(tofersen)获FDA加速批准上市,用于治疗超氧化物歧化酶1(SOD1)突变所致的肌萎缩侧索硬化(ALS)患者。这是首款针对ALS的基因靶向疗法。Tofersen是一种用于治疗SOD1-ALS的反义寡核苷酸药物,可与编码SOD1的mRNA结合,使其被核糖核酸酶降解,从而减少SOD1蛋白的产生。
>>>>全球首款口服粪便微生物疗法:Vowst
4月26日,Seres Therapeutics的口服微生物菌群疗法Vowst(SER-109)获FDA批准上市,用于预防复发性艰难梭菌感染(rCDI)。这是FDA批准的首款口服粪便微生物疗法。SER-109是一种基于细菌孢子的口服微生物菌群疗法,从健康人粪便纯化而来,平均含有大约50种细菌,通过重建肠道菌群,抑制艰难梭菌的生长。SER-109的纯化过程旨在去除不需要的微生物,从而降低病原体传播的风险。此前,FDA已授予SER-109突破性疗法认定和孤儿药称号。
>>>>全球首款RSV疫苗:Arexvy
5月3日,FDA批准GSK的呼吸道合胞病毒(RSV)疫苗Arexvy上市,用于预防60岁以上成人因RSV感染而造成的下呼吸道疾病。这是全球首款获批上市的RSV疫苗。5月31日,辉瑞旗下用于老年群体的RSV疫苗Abrysvo也获得FDA批准上市。8月21日,Abrysvo适应症获FDA扩大至:通过孕妇主动免疫,预防出生至6个月大的婴儿患上RSV相关下呼吸道疾病。
>>>>首款A型血友病基因疗法:Roctavian
6月29日,BioMarin的基因疗法Roctavian获FDA批准上市,是FDA批准的首款A型血友病基因疗法。Roctavian是一款使用AAV5病毒载体递送表达凝血因子VIII(FVIII)转基因的基因疗法。该疗法优势在于可能只需要一次治疗即可获得表达FVIII的基因,因此患者不再需要长期接受预防性凝血因子注射。
>>>>全球首款GPRC5D/CD3双抗:Talvey
8月9日,FDA加速批准强生GPRC5D/CD3双抗Talvey(talquetamab)上市,用于治疗复发或难治性多发性骨髓瘤(MM)成人患者,这些患者先前至少接受过4种治疗,包括蛋白酶体抑制剂,免疫调节剂和CD38抗体。Talquetamab是一款first-in-class现货型双特异性T细胞结合抗体,能同时靶向MM细胞上的GPRC5D和T细胞上的CD3,通过激活CD3阳性T细胞,诱导T细胞对GPRC5D阳性MM细胞进行杀伤。
>>>>首款口服单药PNH疗法:Fabhalta
12月5日,FDA批准诺华的Fabhalta(iptacopan)上市,用于成人阵发性睡眠性血红蛋白尿症(PNH)患者的治疗。这是首个获FDA批准的口服单药治疗成人PNH的药物。Iptacopan是诺华研发的first-in-class、靶向补体旁路途径B因子的口服抑制剂。该产品作用于C5末端通路的上游,同时控制血管内溶血和血管外溶血,弥补了抗C5抗体的不足,同时为患者提供了口服单药的选择。
>>>>首款CRISPR基因编辑:Casgevy
12月8日,Vertex与CRISPR联合开发的CRISPR/Cas9基因编辑疗法Casgevy获FDA批准上市,用于12岁及以上输血依赖性地中海贫血患者或伴有复发性血管闭塞危象的镰状细胞病患者,这些患者没有人类白细胞抗原匹配的造血干细胞供体。这是全球首款获批上市的CRISPR基因编辑药物。就在同日,FDA还批准了蓝鸟生物的一款基因疗法Lyfgenia上市,同样用于12岁及以上伴有复发性血管闭塞危象的镰状细胞病患者的治疗。这是蓝鸟生物推出的第3款基因疗法,据悉该产品定价为310万美元,此前治疗肾上腺脑白质营养不良的eli-cel和治疗β-地中海贫血的beti-cel定价分别为300万美元和280万美元。
2024,我们拭目以待。


