
作者:刘晓武
制药企业数字化转型升级迫在眉睫,阅读此文可帮助您快速梳理数字化平台建设方案,就企业的数字化升级未雨绸缪。

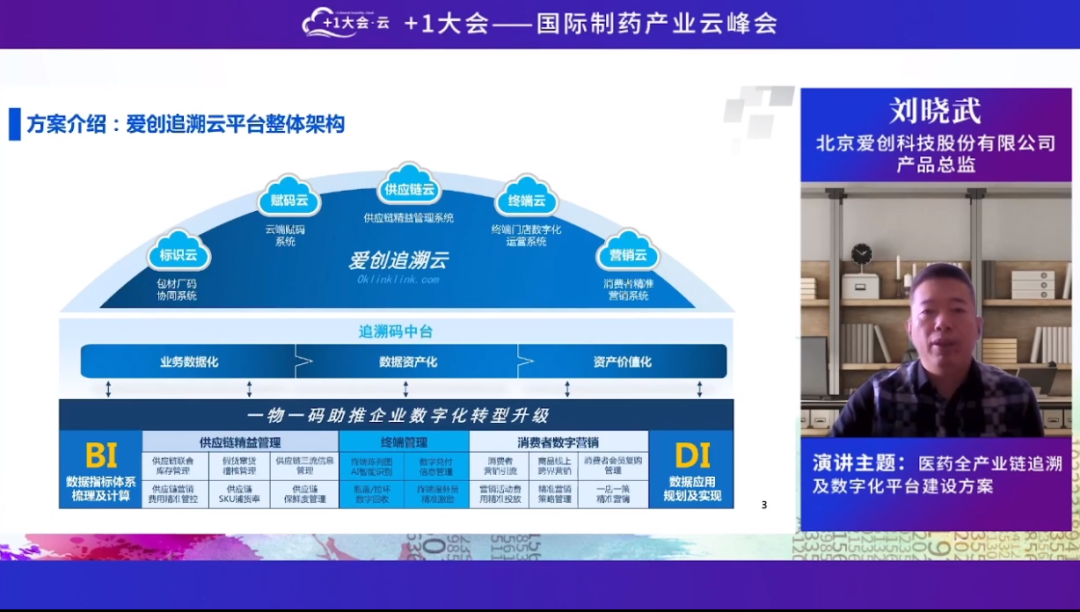
北京爱创科技股份有限公司产品总监刘晓武在+1大会·云—国际制药产业云峰会“连续制造专场论坛”分享了《医药全产业链追溯及数字化平台建设方案》,帮助大家了解数字化平台建设的整个方案细节及项目重点。本文根据嘉宾报告内容整理,经演讲嘉宾本人确认并同意公开分享。
基于100余个项目方案实施的经验,我们发现60%以上的项目不仅完成了DI,还完成了PI管理。整个项目涵盖体外诊断试剂,医美产品、高低值耗材、大型医疗器械设备等六大类。
溯源数字化云平台以进口药实施方案为例,从数据流角度出发,前端通过L4对接国外生产数据,将国内药品生产企业的赋码数据上传到L4平台。L4对接主要涉及的内容包括交易信息、交易历史和交易状态的交换。目前已完成对接SAP、Unitrace,Tracelink等项目,部分通过手动文件上传,部分基于在线接口对接完成。
另外,爱创追溯云可以为药企提供出入库APP、终端赋能系统、防伪防退货小程序、C端腾讯健康药箱等数字化服务程序,通过统一的数据管理对接大型医药物流。通过这种生态对接,解决目前多码并存的业务痛点。同时与NMPA、NHSA等监管平台对接,实时上传追溯数据,例如:对接国家药品(含疫苗)的行动平台。
现在,国家行动平台已经部分上线,集采中标药品、血液、麻醉药品都要向国家系统平台上传相关药品静态数据。四川和海南的省级监管平台陆续上线,其他省正在建设省级平台。三类医疗器械(含体外诊断试剂)要求2022年6月1日前必须实现DI的合规备案。
云赋码通过把所有计算和逻辑的处理放在后台运行,能够减轻前端的设备投入压力,而前端、产线端更多是工业相机的信息采集。云赋码方案较传统的赋码方案具备以下优势:设备投入少、加快项目实施进度,增强产线的稳定性、易维护、生产可视化、可进行产线动态监控等。基于现在设备更新和网络升级的频率,未来云赋码方案是新趋势。
在进口药方面已经实现对接国家医保核查鉴证平台,一些集采中标药品,国家要求在部分试点城市的试点医院完成与医保核查鉴定平台的对接。主要目的是监管中标的药品在医院出入库、医院结算价格和出入库一段时间内的匹配度,进而监管惠民政策的落地执行情况。以西安杨森为例,杨森进口药在武汉市雅馨医院完成对接了核查鉴证平台,爱创追溯云帮助杨森在新的合规要求下,成功实现供应链药品的正常出入库和在医保结算和药店终端的对码。目前在医院内有不同的编码,所以想统一通过医保码来完成监管。
爱创追溯云可完成各种编码之间的映射及对码的监管工作。对于企业需要掌控整个实施过程的质量,控制进度的需求,可提供基于CSV全生命周期各个过程的专业计算机认证文件的输出,根据具体要求输出不同阶段和类别的认证文档。
药品序列化是提供码的申请下载、包材赋码、产线激活、多级关联的整体解决方案。产品序列化的过程当中,采集率高和准确的关联关系是所有数字化建设的基础。
数字化生产运用工业自动化、智能识别、多层信息加密和软硬件集成的光机电算技术,为每一件商品创造唯一的ID,然后建立包装关联。
数字化渠道有核心产品出入库的APP,我们推荐对扫码量大、精度要求高的企业使用PD专业设备。如果是扫码量少的企业,推荐使用可以进行多码兼容的小程序,市场上原有的老电子监管码,新的GS1 等都能兼容识别。数字化终端的小程序可以进行终端赋能,为药店或者私人诊所进行终端精细化管理,激励促销员,不断提高收益。
在患者终端服务有腾讯健康药箱,它的主要功能是提高患者用药依从性。比如:它可以提高慢性病患者的用药依从性、为患者提供权威易懂的疾病和用药科普信息。整合医学服务进行用药、问药、购药一站式服务。
健康药箱分成四个版本,大众版、专业版、企业版、创新版。大众版具备各种功能,它是基于腾讯全民13亿人超级入口的应用,扫普通的追溯码就可以实现一级跳转,进行品牌宣传。在线购药问药,还有一些患者端的粘性服务——例如“我的药箱”、“用药提醒”等应用。专业版、企业版、创新版在大众版的基础上增加了数字化运营,包括一些定制化功能,充分调动企业资源,打造以患者为中心的一站式数字化服务C端程序。
患者端的数字化服务是通过患者标签化的数据,加强入库认知,采集C端的数据与B端进行互动,实现医患互动,建立购药闭环管理。根据患者的分类和患者画像的数据反馈,生产端数据和服务可以精准触达患者。
进口药的UDI项目普遍以满足中国法规和完成自身数字化为重点。其中自身数字化的需求是指掌握药品在国内的销售情况、库存情况,对于一些新投放的药品可以通过追溯系统快速建立国内和国外的全产业链数据衔接,然后形成一个全链条可追溯的架构。
杨森是中国第一个基于GS1实现全产业追溯的案例。产品在比利时生产,有9个SKU进入中国,在中国有5个第三方物流,然后发到西安、北京、广州和上海四个分仓,再到60个经销商和400个终端,最终到达患者。
进口药存在多码并存的情况,PDA出入库应用既可以识别GS1码、也可以识别原来的电子监管码,实现多码兼容,完成出入库扫码,最后把流向数据传给追溯平台,形成药品流向、流量、流速的全面管理。
出口药的UDI项目核心需求相对比较简单,出口药主要完成L1到L3的工作,在国内完成产品序列化,通过L3对接国际L4即可。出口药方案的核心是要做好赋码产线上光学机电设备,然后实现一物一码的采集关联,上传到最终追溯系统,最后由EDI service对接国际上的Tracelink、SAP等L4平台。这一部分的难点在于,出口目的地国家和地区不同,赋码的方式位置、标签的尺寸也存在差异,赋码方式需要进行适配。
UDI项目不管是药品还是医疗器械,首要需求是合规。企业的自身数字化需求是DI+PI,实现医疗器械一物一码的管理和整个生产企业出入库和流向的管理,也有部分企业存在防伪防窜货的需求。未来,经营企业和使用单位都会建设相关的追溯系统。监管部强制要求三类医疗器械及体外诊断试剂在2022年6月1号前要完成DI上传。同时,预计在2022年6月1日之后,我国也会模仿欧洲和美国相继进行三类、二类和一类的上线。





