作者:阳光
10月14日,CDE官网显示,博安生物的地舒单抗注射液(LY06006 / BA6101)上市申请获药监局受理。这是国内第二个申报上市的地舒单抗生物类似药。
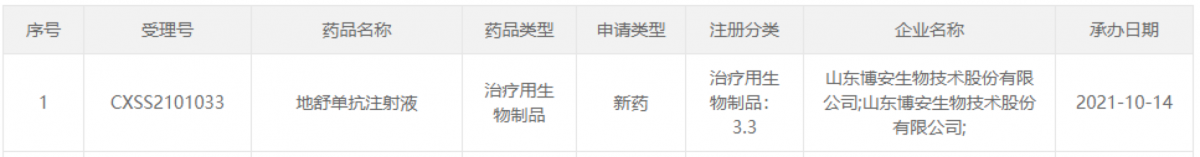
BA6101是一种IgG2全人源单克隆抗体,通过抑制RANKL与其受体RANK的结合,减少破骨细胞形成、功能和存活,从而降低骨吸收、增加骨量、改善皮质骨或松质骨强度。
BA6101的原研是由安进研发的地舒单抗,商品名为Xgeva(70 mg/ml)和 Prolia(60 mg/ml)。2010年5月在欧盟上市,同年6月在美国上市。2019年5月,地舒单抗在中国获批上市,商品名为安加维,用于治疗骨巨细胞瘤。此后在国内陆续扩展新的适应症,分别是骨折高风险的绝经后妇女的骨质疏松症和预防实体瘤骨转移及多发性骨髓瘤引起的骨相关事件(SRE)。

地舒单抗注射液在全球范围呈现广阔的市场前景。根据医药魔方NextPharma数据库,安加维2020年的全球销售额超46亿美元。值得注意的是,地舒单抗的核心专利到期时间是2025-2026年。(见:未来10年专利到期重磅药物(12)——地舒单抗)
Prolia (地舒单抗)销售额
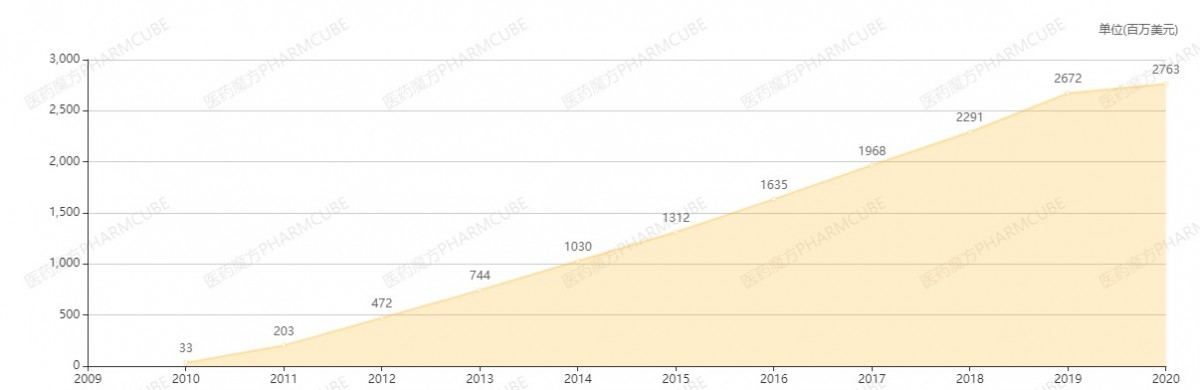
Xgeva (地舒单抗)销售额
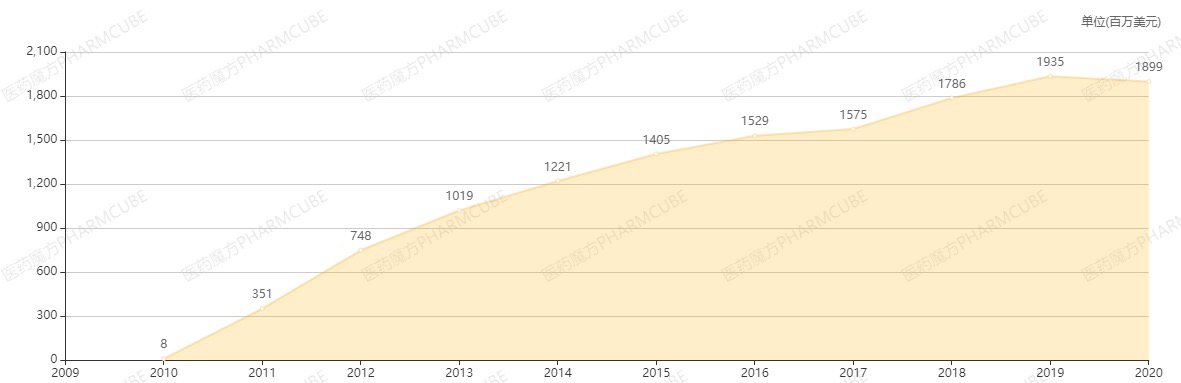

Xgeva (地舒单抗)销售额

截止目前,国内已有2款地舒单抗生物类似药申报上市。今年8月30日,齐鲁制药的地舒单抗注射液上市申请获受理。除此之外,处于临床III期阶段的有康宁杰瑞、百迈博制药、泰康生物。



 上一篇
上一篇 下一篇
下一篇




